PLAY250
+500% к Депозиту!
1win – это не просто букмекерская контора, это целая вселенная азарта и выигрыша. 1win – это не просто букмекерская контора, это целая вселенная азарта и выигрыша.
В 1win каждый найдет что-то для себя:
- Фанаты спорта смогут испытать свои знания и интуицию, делая ставки на сотни матчей в десятках дисциплин.
- Любители азарта погрузятся в мир виртуальных казино, где тысячи слотов и настольных игр зажгут огонь в их глазах.
- Те, кто жаждет испытать удачу, смогут сделать ставку на киберспорт, покер или лотерею, бросив вызов фортуне.
1win – это не просто сайт, это:
- Эмоции, которые захлестывают с каждой ставкой.
- Азарт, который бурлит в крови.
- Волнение, которое заставляет сердце биться чаще.
- Радость от каждого выигрыша.
 Название Название |
1win |
 Год создания Год создания |
2016 |
 Приветственный бонус Приветственный бонус |
До 500% на первый депозит |
 Промокод Промокод |
PLAY250 |
 Виды игр Виды игр |
Казино, Беттинг, Покер |
 Приложение Приложение |
Android, iOS |
 Лицензия Лицензия |
Лицензия Кюрасао |
 Другие названия Другие названия |
1 вин, 1xwin, ван вин, вин 1 |
 Языки Языки |
Мультиязычный: 18 языков |
 Приложение Приложение |
Android, iOS (1win apk, iOS ярлык) |
 Поддрежка Поддрежка |
24/7 |
 E-mail поддержки E-mail поддержки |
[email protected] |
Что делает 1win особенным?
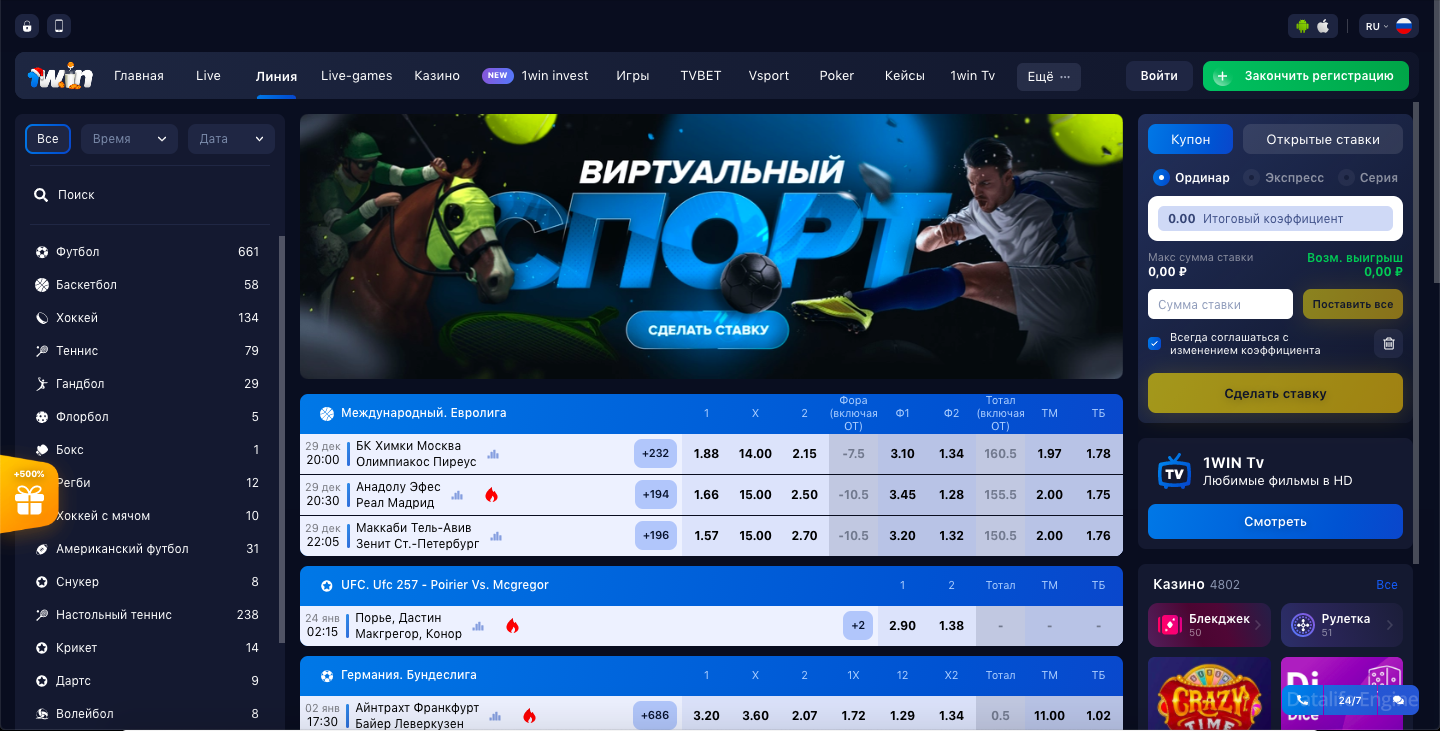
- Широкая линия ставок: 1win предлагает своим игрокам широкий выбор ставок на более чем 30 видов спорта, включая футбол, хоккей, баскетбол, теннис, киберспорт и многое другое.
- Высокие коэффициенты: 1win предлагает своим игрокам одни из самых высоких коэффициентов на рынке.
- Быстрые выплаты: 1win выплачивает выигрыши своим игрокам максимально быстро.
- Щедрые бонусы: 1win предлагает своим игрокам щедрые бонусы и акции.
- Удобный интерфейс: Сайт и приложение 1win имеют удобный и понятный интерфейс.
- Круглосуточная служба поддержки: Служба поддержки 1win работает круглосуточно 7 дней в неделю.
1win – это букмекерская контора, которая по праву считается одной из лучших на рынке. Она предлагает своим игрокам все, что нужно для успешных ставок: широкий выбор ставок, высокие коэффициенты, быстрые выплаты, щедрые бонусы и удобный интерфейс.
Ставки на спорт в конторе 1вин
Когда речь заходит о ставках на спорт, букмекерская контора 1вин превращается в настоящую арену азартных сражений, где каждый фанат спорта может проявить свою проницательность и страсть к игре. В этом мире ставок вас ожидает множество спортивных дисциплин, словно звезды на небосклоне, каждая из которых сверкает и притягивает внимание своим уникальным блеском.
Среди многообразия доступных направлений 1вин выделяет наиболее популярные виды спорта, такие как футбол, который неизменно собирает миллионы поклонников у экранов в ожидании захватывающих матчей и непредсказуемых исходов. Баскетбол, с его динамичными перепадами и виртуозным мастерством игроков, также занимает почетное место среди предпочтений бетторов. Теннис, хоккей, волейбол – каждый из этих видов спорта представлен в полном объеме, предоставляя богатый выбор турниров и игр.
Не обошла стороной 1вин и более экзотические дисциплины, такие как крикет, дартс или флорбол, давая возможность истинным ценителям найти свой уголок страсти и экспертизы. Именно здесь вы можете испытать свою интуицию, делая ставки на исходы, которые кажутся вам наиболее вероятными, основываясь на анализе статистики, формы команд и индивидуальных достижений спортсменов.
Здесь вы не просто делаете ставки – вы становитесь частью каждой игры, каждого соревнования, живя вместе с командами каждый момент на пути к победе.
Букмекерские конторы для привлечения новых клиентов и поддержания интереса постоянных игроков постоянно совершенствуют свою программу лояльности. Однако все организации обычно увеличивают количество акционных предложений и не задумываются об увеличении суммы выигрыша. Организация 1win решила пойти по другому пути. Так, например, букмекер может предложить для своих клиентов приветственный бонус на пополнение счета в размере до 500%. Получение, которого распределено на четыре первых депозита.
В данной статье будет подробно рассмотрено бонусная программа 1win, а также условия отыгрыша и получения бонусов. Для того чтобы получить любой из существующих бонусов, потребуется в первую очередь провести регистрацию. Без прохождения которой поучаствовать в акционных предложениях не получится. Во время заполнения анкеты можно ввести специальный промокод, который обеспечивает возможность увеличения приветственного бонуса. Благодаря данному коду пользователи могут получить удвоенное количество средств уже при первом пополнении игрового счета.
В современном мире азартных игр 1win официальный сайт выделяется своей доступностью и удобством использования. Для того чтобы начать пользоваться всеми преимуществами платформы, первым делом необходимо пройти процесс регистрации. 1 win регистрация предлагает пользователям два основных метода создания аккаунта, которые отличаются своей простотой и скоростью.
- Первый метод — это классическая регистрация с использованием электронной почты. Пользователю необходимо указать свою электронную почту, придумать пароль, а также ввести промокод PLAY250 для получения специальных бонусов на начальном этапе. Этот метод хорош тем, что вы всегда сможете восстановить доступ к своему аккаунту через электронную почту.
- Второй метод — регистрация через социальные сети. 1вин регистрация предлагает возможность создать аккаунт, используя профили в популярных социальных сетях, что значительно ускоряет процесс регистрации. Выбрав этот способ, пользователь сможет войти на сайт, используя свои учетные данные из социальной сети, что делает 1win вход еще более удобным.
После успешной регистрации важным шагом является верификация аккаунта. Этот процесс заключается в подтверждении вашей личности и является обязательным для гарантии безопасности ваших финансовых операций на платформе. Для верификации вам потребуется предоставить сканы документов, подтверждающих вашу личность. Эта мера предотвращает возможные мошеннические действия и обеспечивает защиту аккаунтов пользователей.
1 вин вход на сайт после регистрации и верификации становится максимально простым и безопасным. Пользователи могут с уверенностью пользоваться всеми предложениями платформы, наслаждаясь азартными играми, ставками на спорт и другими развлечениями.
Делать ставки на спортивные мероприятия, крутить слоты в казино и следить за результатами игр можно не только сидя у стационарного компьютера или ноутбука. Гораздо удобнее делать это с телефона или планшета. Все что вам нужно - скачать 1win на андроид.
Технические характеристики:
| Разработчик | 1win |
| Размер | 14 mb |
| Требуемая версия ОС | 4.1+ |
| Формат | apk |
| Язык | Русский |
Мобильное приложение 1вин на вашем устройстве позволит заключать пари в любое время, в любом месте. Процесс скачивания apk файла не занимает большого количества времени, а установка проста и доступна для каждого пользователя.
Как скачать и установить 1win apk на андроид
Каждый беттор пользующийся гаджетом на операционной системе Андроид может скачать приложение 1win на свое устройство. Apk файл доступен на нашем официальном сайте. Кликните по соответствующей кнопке в шапке сайте, после чего начнется загрузка приложения на ваше устройство. Для инсталляции скаченного архива необходимо выполнить следующие действия:
В сфере онлайн-гемблинга постоянно возникают препятствия в виде блокировок официальных сайтов на территории некоторых стран. 1win официальный сайт не является исключением из этого правила и может быть недоступен для прямого посещения. В таких случаях на помощь приходят 1win зеркало сайты альтернативные адреса, которые предоставляют полный доступ к функционалу основного сайта.
Использование 1вин зеркало – это проверенный и безопасный способ обхода блокировок. Основное преимущество зеркал заключается в их способности предоставить неизменный пользовательский опыт, несмотря на ограничения доступа к основному домену. Для нахождения 1win зеркало рабочее на сегодня прямо сейчас, рекомендуется обратить внимание на шапку официального сайта, где обычно размещаются актуальные ссылки.
Не стоит забывать о важности проверки подлинности зеркала, поскольку интернет пестрит фальшивыми сайтами, целью которых является мошенничество. Одним из способов удостовериться в надежности 1xwin зеркало является поиск отзывов в интернете или обращение к официальным источникам информации.
Благодаря зеркалам, пользователи могут продолжать наслаждаться игровым процессом, не волнуясь о блокировках и ограничениях.
1WIN сегодня это не только популярный ресурс онлайн-ставок на спорт, но известное online казино. Здесь каждый может попробовать свои силы на множестве игровых автоматов от топовых производителей. К услугам клиентов обширный перечень настольных игр, а также возможность сразиться с реальными дилерами. Официальный сайт 1win казино это достойная и отличная рекомендация, подтвержденная многолетней надежной репутацией. Деятельность казино регламентируется на основании лицензионного соглашения.
ОФИЦИАЛЬНЫЙ САЙТ КАЗИНО 1WIN
Казино 1win действует на основании лицензии о. Кюрасао согласно законодательству указанного гражданства. Поставщиками программного обеспечения для 1 WIN являются такие гиганты индустрии как Yggdrasil,Edorphina, Amatic, Play'n GO, GamART, EGT, Playson, и аналогичные ТОП разработчики. Игрокам казино 1 вин предложен широкий ассортимент в пределах 1000 игр. Это и стандартные ставки на спорт, телевизионные игры, живые игры, варианты игр в мобильном приложении, а также популярнейший ежемесячный покерный турнир!
Веб-сайт букмекера 1win выстроен разработчиками максимально понятно, интерфейс прост благодаря удобной навигации с иконками. Сайт отличает качественное юзабилити, являясь ключевым элементом стратегии 1win. Техническая поддержка работает в режиме 24/7, гарантируя круглосуточные ответы на вопросы клиентов (по email, в чате с оператором, по телефону). Диалоги осуществляются на нескольких языках по всему миру.